Сложные эфиры: что это такое и их применение
Когда вы пьете лимонад и чувствуете вкус банана или груши — вы имеете дело со сложными эфирами. В химии их классифицируют по свойствам, образованию класса соединения, по названиям.
Сложные эфиры – что это, определение
Сложный эфир является органическим соединением. В нем водород заменен на углеводородное соединение в карбоксильной группе. Эти химические элементы получают из карбоновых кислот, смешанных со спиртом.
Немецкий химик Леопольд Гмелин впервые назвал подобные соединения сложным эфиром. На немецком это словосочетание звучит, как «essigäther». В дословном переводе оно означает уксусный эфир.
В записях на уроках химии вы, наверное, уже сталкивались с формулами сложных эфиров. Формулы записывают следующим образом: «RCO2R'». Здесь литера «R» означает углеводородную часть карбоновой кислоты, а литера «R» с апострофом после нее говорит о присутствии спирта. Есть еще одна формула, присущая только ортоэфирам. Она записывается следующим образом: С(OR)4 и R'С(OR)3.
Ортоэфиры тоже относятся к сложным эфирам и представляют собой эфиры несуществующих в природе кислот: ортоугольной и ортокарбоновой. Это гидратированные формы угольной и карбоновой кислот.
Сложные эфиры рассматривают как производные спиртов, тиолов, фенолов, селенолов.
Номенклатура сложных эфиров
Сложные эфиры классифицируют по систематической номенклатуре и по рациональной номенклатуре. При написании названия сложного эфира по систематической номенклатуре используют название спирта в соединении с кислотным остатком и добавляют суффикс «ат». Например, метилформиат.
При написании названия сложного эфира по рациональной номенклатуре используют название кислоты, радикал спирта, суффикс с окончанием «овый» и слово «эфир». Например, муравьинометиловый эфир.
Изомерия сложных эфиров
Изомерия сложных эфиров возможна. Например, есть изомерия углеродного скелета радикала кислоты и радикала спирта, если присутствуют 3 и больше 3 атомов углерода.
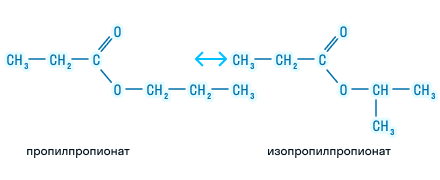
Также есть изомерия положения функциональной группы сложных эфиров.
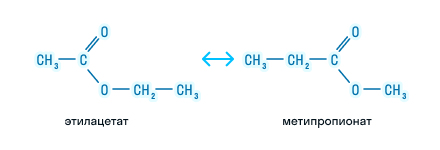
Если химические соединения сложных эфиров содержат непредельную кислоту, либо непредельный спирт, то будут допустимы еще два типа изомерии. Это изомерия положения кратной связи, а также цис-изомерия и транс-изомерия.
Физические свойства сложных эфиров
Так как сложные эфиры подразделяют на низшие карбоновые кислоты и простейшие спирты и высшие карбоновые кислоты, то в соответствии со своей природой они имеют те или иные физические свойства. Например, эфиры простейших спиртов и низших карбоновых кислот представляют собой соединения с приятным фруктовым запахом. Они легко воспламеняются, не имеют цвета. Такие сложные эфиры являются летучими веществами.
Сложные эфиры высших карбоновых кислот имеют другое строение. Они представляют собой твердые вещества. Эти химические соединения не имеют запаха и практически бесцветны.
Есть сложные эфиры низших минеральных кислот. К ним относят алкилсульфиты, алкилсульфаты, алкилбораты. Химические соединения представляют собой маслянистые жидкости с приятным запахом.
Сложные эфиры отличаются по температуре кипения. Например, химические вещества от низших спиртов имеют значительную низкую температуру кипения, чем сложные эфиры кислот. Все сложные эфиры практически не растворяются в воде. Органические растворители растворяют сложные эфиры за несколько минут.
Соединения легко вступают в реакцию с аммиаком. В результате образуются амиды. Таким образом получаются маргарины из растительных масел.
Химические свойства сложных эфиров
В нейтральной среде сложные эфиры показывают себя как устойчивые соединения. Но, если на них воздействовать повышением температуры в присутствии кислот или щелочей, то они легко разлагаются.
Если присутствуют кислоты, то этерификация протекает как обратная реакция. Во время этой реакции образуется спирт и карбоновая кислота. Например, при гидролизе метилацетата получается уксусная кислота и метанол.
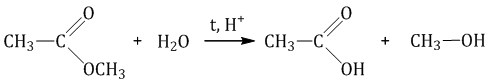
Если воздействовать на эфир щелочью, то образуется соль карбоновой кислоты и спирт. Например, этанол и формиат натрия при гидролизе этилформиата.
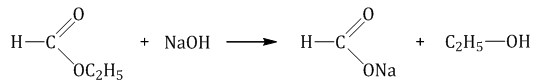
Способы получения
Сложные эфиры получают путем этерификации. Этерификация — это химическая реакция, в результате которой образуется сложный эфир. Узнать, что у вас получилось именно данное соединение можно по легкому фруктовому запаху.
Для получения реакции этерификации смешивают кислоту и спирт. В результате получается молекула кислоты, в которой атом водорода замещается углеводородным радикалом. Например, создают этерификацию карбоновых кислот спиртами.
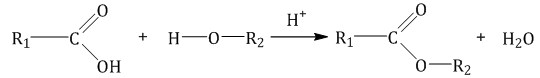
Также используют реакцию карбоновых кислот с галогеналканами. Ниже на формуле представлено получение метилацетата путем соединения ацетата натрия с хлорметаном. Таковы химические свойства сложных эфиров.
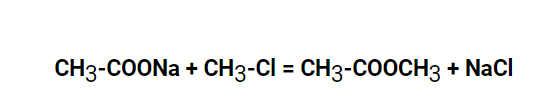
Также возможно восстановление сложных эфиров. В этом случае получается смесь спиртов. Восстановление происходит путем разрыва связи С-О карбоксильной группы. Ниже мы видим, что этилбензоат восстановлен гидридом литий-алюминия до бензилового спирта и этанола.
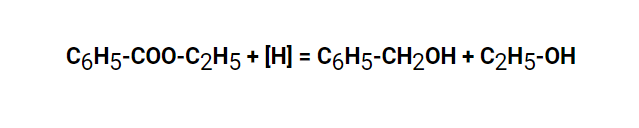
Сложные эфиры в природе – и их применение
Сложные эфиры в природе являются ключевыми компонентами жиров и восков. Например, эфиры фосфорной кислоты являются органическими фосфатами. Они входят в ДНК, РНК и фосфолипиды. Без них жизнедеятельность организма будет затруднена.
Сложные эфиры используют в органическом синтезе. Из них создают инсектициды, гербициды, смазки, пропитки для кожи и бумаги, моющие средства, глицерин, нитроглицерин, олифу, масляные краски, синтетические волокна и смолы.
Сложные эфиры используют как добавку к моторным маслам. Фруктовые эссенции для лимонадов, отдушки, косметические ароматизаторы — все это является сложными эфирами. Растворители лаков, красок, смол тоже относят к соединениям сложных эфиров.
Задачи – примеры и решение
Давайте посмотрим на примеры задач и приведем методы их решения.
Задача № 1 имеет следующее содержание: Сложный эфир подвергли гидролизу с щелочью. Масса эфира до гидролиза была равна 14,8 грамма. В результате получили 19,6 грамма калиевой соли предельной одноосновной карбоновой кислоты и 6,4 грамма спирта. Нам нужно узнать молекулярную формулу сложного эфира.
Решение будет таково:
- Для начала нужно составить уравнение реакции.
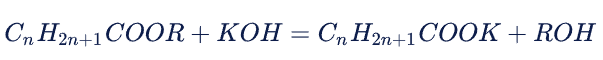
- Затем нужно найти массу и количество гидроксида калия.
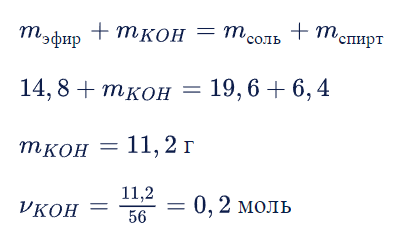
- Теперь необходимо прописать уравнение реакции.

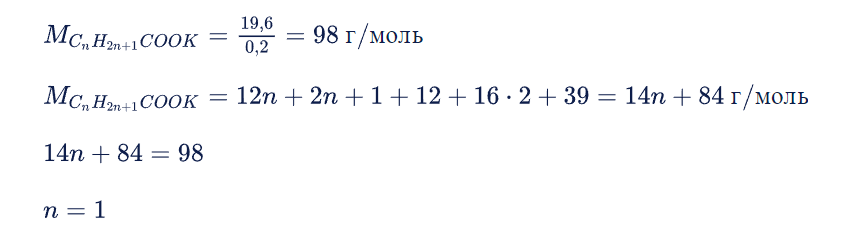
Из решения задачи видим, что формула соли записывается следующим образом: CH3COOK, а формула кислоты CH3COOH.
Снова нужно обратиться к уравнению.
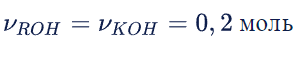
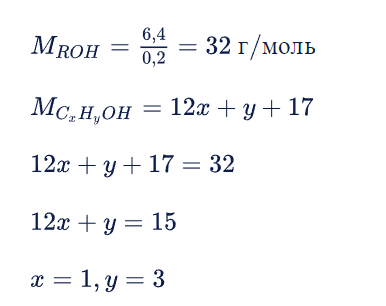
В результате формула спирта будет записана как CH3OH. Отсюда узнаем формулу сложного спирта: CH3COOCH3.
FAQ
Что такое фруктовые эфиры? Они тоже относятся к сложным эфирам?
Да, фруктовые эфиры относят к сложным химическим соединениям и называют эфирами. Они представляют из себя жидкости, молекулы которых имеют не более 8 атомов углерода. Когда вы понюхаете, то почувствуете легкий аромат. Такие соединения состоят из одноатомных спиртов и карбоновых кислот. Они также плохо растворяются в воде. Однако легко реагируют с галогенами, щелочами, спиртами и кислотами.
Можете подсказать примеры жиров сложных эфиров?
Да. Например, оливковое масло. Это смесь глицерина с остатками пальмитиновой, стеариновой, олеиновой, линолевой кислот.
Возможна ли реакция галогенирования сложных эфиров?
Да, возможна при кратных связях. Если кратные связи отсутствуют, то не будет подобной реакции. Один из примеров подобной реакции: CH2=CH-C(O)-O-CH3 + Br2 → Br-CH2-C(Br)H-C(O)-O-CH3.
Могут ли сложные эфиры содержать остатки минеральных или карбоновых кислот?
Да, могут. Например, если взять тоже самое оливковое масло, то оно содержит остатки кислот.
Вывод
Теперь вы познакомились со сложными эфирами, узнали, как их классифицируют и как решают задачи по поиску формулы спиртов и других химических соединений. Эти знания могут пригодится на экзаменах по химии в 9 и 11 классах.
